用于体外血液毒性测试的HemaTox™培养基和补充剂
为什么使用 HemaTox™ 试剂盒?
- 本方法已通过与体外IC50测定现行金标准——集落形成单位(CFU)检测法的对比验证。
- 经优化的无血清培养基及补充剂可实现高效扩增,确保实验结果一致性。
- 测试化合物可在培养起始阶段加入以观察对祖细胞的影响,或在培养后期加入以研究对分化程度更高细胞的作用。可以使用不同的检测方法,例如流式细胞术。
数据

图1. HemaTox™试剂盒通用操作步骤
*如果使用的是已预先富集的CD34+细胞,可以省略细胞分离步骤。

图2. 流式细胞术图显示CD34+造血干细胞使用HemaTox™红系、髓系和巨核细胞试剂盒培养后产生的细胞
(A)人 CB CD34+ 用 (B) HemaTox™ 红系、(C) 髓系和 (D) 巨核细胞试剂盒按照上述方案培养后的细胞。完成既定培养周期后,分别收集细胞并进行表面蛋白标记:红系(CD71与GlyA)、髓系(CD13与CD15)或巨核系(CD45与CD41)特异性表达蛋白的染色
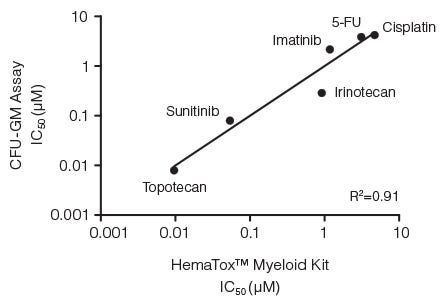
图3. CFU-GM 集落形成实验与 HemaTox™髓系试剂盒在96孔板液体培养体系检测六种药物 IC50 值的相关性分析
采用MethoCult™培养基进行粒-巨噬细胞集落形成单位(CFU-GM)实验,同时使用HemaTox™髓系试剂盒进行液体培养,对人骨髓 CD34+ 细胞进行培养。将两种方法测得的 IC50 值分别绘制于X轴与Y轴,结果显示其具有高度相关性(决定系数R²=0.91)。

图4. 用 HemaTox™ 红系、髓系和巨核细胞试剂盒鉴定血液毒性的谱系特异性差异
结果显示:使用HemaTox™红系(灰色)、髓系(金色)和巨核系(橙色)试剂盒对人骨髓CD34+细胞进行药物测试获得的平均IC50值。多数药物对各细胞谱系毒性相似,但舒尼替尼(Sunitinib)等药物对红系祖细胞分化的毒性约为巨核系祖细胞的100倍,对髓系祖细胞分化的毒性介于两者之间。垂直线表示均值标准误差(SEM)(n=4-8)。
合同检测服务
整合专业资源与技术专长可有效提升药物研发管线效率。我们的合约检测服务(CAS)团队通过优化培养基体系、预验证细胞资源及专业技术支持,在原代细胞检测平台中实现候选治疗药物的高效筛选

 EasySep™小鼠TIL(CD45)正选试剂盒
EasySep™小鼠TIL(CD45)正选试剂盒







 沪公网安备31010102008431号
沪公网安备31010102008431号